Informe de Encuentro científico mundial sobre miopía. Expertos científicos y clínicos de la OMS y el Instituto de la Visión Brien Holden revisan los principales problemas de la miopía.
La miopía es la principal causa de discapacidad visual moderada y grave (42%) y una causa importante de ceguera (3%). La mayoría de los errores de refracción a distancia son causados por la miopía; Se espera que la prevalencia mundial de la miopía aumente del 27% de la población mundial en 2010 al 52% en 2050.
Tabla de contenidos
Introducción
La prevalencia de la miopía y la miopía magna aumentan a nivel mundial a un ritmo alarmante, con aumentos significativos en los riesgos de discapacidad visual por afecciones patológicas asociadas con la alta miopía/miopía magna, que incluyen daño retiniano, cataratas y glaucoma. El impacto de la miopía es difícil de determinar, porque no hay definiciones estándar de miopía y miopía alta, y el reconocimiento de que la miopía puede conducir a un deterioro de la visión está limitado por la ausencia de una categoría definida de enfermedad de la retina miope que causa un deterioro permanente de la visión.
En el año 2015 la preocupación y el compromiso del Gobierno australiano por el impacto actual y futuro de la miopía, así como la atención insuficiente que recibía el problema de la discapacidad visual asociada con la miopía, en términos de evaluación de prevalencia, intervenciones preventivas y posible tratamiento, llevó a las autoridades sanitarias australianas a solicitar la participación de la OMS en una reunión científica internacional sobre miopía a cargo del Brien Holden Vision Institute (BHVI). Se compartieron los resultados más recientes de investigaciones concluyentes sobre los temas centrales revisando la evidencia publicada, analizando y acordando definiciones sobre la base de evidencia científica y práctica médica actual, revisando datos epidemiológicos sobre morbilidad y donde se discutieron las consecuencias sociales y económicas para los niños, los ancianos y la sociedad (Anexo 2). Se prestó especial atención a la evidencia sobre estrategias para reducir el aumento evaluado y proyectado en la prevalencia de miopía y su aplicabilidad en la salud pública más allá de los entornos de investigación
Al final de la reunión, las definiciones y la terminología se pusieron a disposición para su consideración, en el marco de la undécima revisión de la Clasificación Internacional de Enfermedades 10, y las conclusiones sobre políticas de salud pública basadas en evidencia y recomendaciones para investigaciones adicionales fueron presentado como contribución a la resolución WHA66.4 de la Asamblea Mundial de la Salud sobre un plan de acción mundial sobre salud ocular universal para 2014-2019 11.
Prevalencia mundial de la miopía
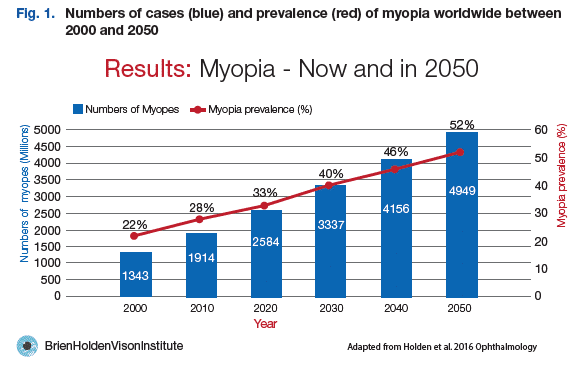
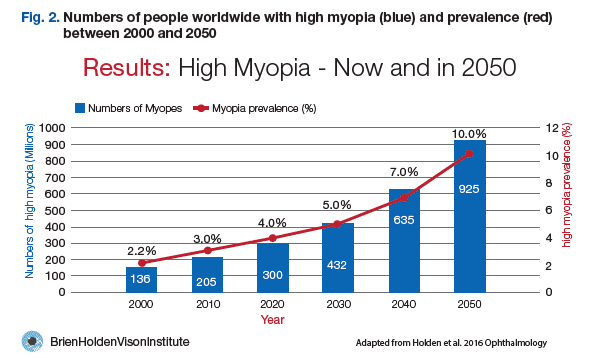
Se estima que, en 2010, la miopía y la miopía magna afectaba al 27% (1893 millones) y al 2.8% (170 millones) de la población mundial, respectivamente. Según estudios publicados, la prevalencia de la miopía es más alta en el este de Asia, donde China, Japón, la República de Corea y Singapur tienen una prevalencia de aproximadamente el 50%, y menor en Australia, Europa y América del Norte y del Sur (2).
Las proyecciones preliminares basadas en estos datos de prevalencia y las cifras correspondientes de la población de las Naciones Unidas (12), y teniendo en cuenta los efectos de la edad y el tiempo, indican que la miopía y la miopía alta afectarán al 52% (4949 millones) y al 10,0% (925 millones), respectivamente, de la población mundial para 2050 (2) (Figs. 1 y 2).
La miopía como causa de la discapacidad visual y ceguera
Se ha informado que el error refractivo no corregido es la primera causa de discapacidad visual en el mundo (1), y la miopía mal corregida es la causa más común de discapacidad visual, según se juzga por la presentación de una agudeza visual deficiente.
La miopía se asocia con mayores riesgos de glaucoma y catarata, pero puede proteger contra la degeneración macular relacionada con la edad y la retinopatía diabética.
La DMM es la causa más común de discapacidad visual en pacientes con miopía, ya que el 10% de las personas con miopía patológica desarrollan DMM (debido a la neovascularización coroidea). Actualmente, la neovascularización coroidea en la DMM se maneja mediante el tratamiento con agentes antivasculares del factor de crecimiento endotelial, pero quedan muchas preguntas con respecto a los regímenes de tratamiento, monitoreo, seguimiento y resultados a largo plazo.
Terminología y clasificación
Miopía, Miopía Magna y Miopía patológica
Como en esos momentos no existía un umbral acordado internacionalmente para la miopía o para la miopía alta, Se vio necesaria una definición operativa para los anteriores términos y que los resultados de los estudios basados en la población se pudieran realizar con los mismos criterios en diferentes países. Se deben realizar estudios longitudinales de miopía alta y miopía patológica para cuantificar el riesgo de afecciones que amenazan la vista debido a la miopía magna.
Los participantes acordaron que una clasificación de miopía alta como ≤ –5.00 D es la mejor definición, ya que una persona que tiene miopía sin corregir –5.00 D tiene una agudeza visual de 6/172 (10), que es mucho peor que el umbral de ceguera (<3/60 en el mejor ojo) (35). Se acordó que la miopía patológica es una miopía alta con anomalías del fondo del ojo relacionadas con la miopía, como la DMM y el glaucoma.
Degeneración macular miópica (DMM)
La DMM es una causa importante de discapacidad visual en la miopía alta. Se utilizan varios términos, incluyendo DMM, maculopatía miope, retinopatía miope y neovascularización coroidea miope. Aunque otras características de la miopía patológica pueden causar discapacidad visual, se debe utilizar el mismo término en todos los estudios y en la práctica clínica para garantizar una clasificación y evaluación inequívoca de la discapacidad visual debido a la alta miopía. La DMM incluye signos de atrofia coriorretiniana difusa, atrofia coriorretiniana irregular, grietas de laca, neovascularización coroidea y atrofia macular relacionada en presencia de miopía superior.
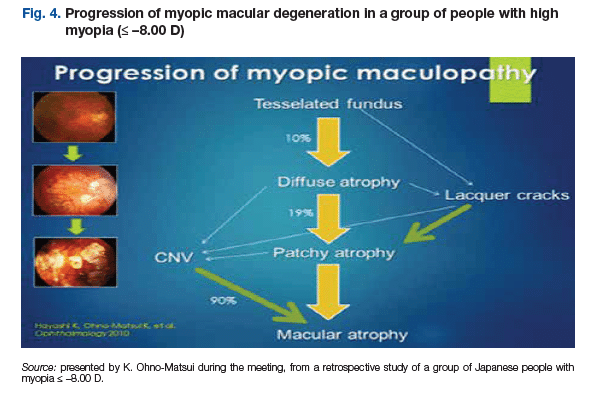
La DMM se desarrolla en presencia de alta miopía, con cambios iniciales en la retina que conducen a un fondo teselado, que luego puede convertirse en atrofia difusa o grietas de laca, atrofia irregular o neovascularización coroidea y finalmente DMM (Fig.4).
Impacto de la miopía
El error de refracción a distancia no corregido se estimó para 2013 en 108 millones de personas en todo el mundo (1). Es la principal causa de discapacidad visual moderada y grave (42%) y una causa importante de ceguera (3%) (1). La mayoría de los errores de refracción a distancia son causados por la miopía; Se espera que la prevalencia mundial de la miopía aumente del 27% de la población mundial en 2010 al 52% en 2050 (2). Si no se aborda la prevalencia creciente de miopía, se puede esperar un aumento similar en el error refractivo no corregido. Estas proyecciones se basan en supuestos conservadores y, dada la relación publicada entre el nivel de educación y la miopía, una mayor provisión de educación podría aumentar notablemente estas tendencias.
Este aumento podría dar como resultado las siguientes consecuencias:
- Pérdida global de productividad
- Probabilidad que el costo de la atención aumente significativamente, y se verá exacerbado por un aumento aún mayor en la prevalencia de miopía alta, del 2.8% (190 millones de personas) al 9.7% (924 millones de personas) para 2050 (2), lo que representa un aumento de 4.9 veces en la miopía alta.
- Pérdida de calidad de vida y desarrollo personal.
- El aumento en la prevalencia de miopía alta eventualmente conducirá a un aumento en la miopía patológica y, por lo tanto, ceguera y discapacidad visual permanente, con un aumento de la presión asociada en los servicios oftalmológicos y de baja visión.
Los participantes acordaron sobre la base de la evidencia de que la miopía justifica los esfuerzos sinérgicos nacionales e internacionales, ya que los costos y las implicaciones para la salud pública son enormes y a menudo se subestiman.
Evidencias para la causa de la miopía
Influencias ópticas y ambientales
Se han identificado varios factores ópticos y ambientales como posibles causas del inicio y la progresión de la miopía, actuando individualmente o en combinación.
- Desenfoque hipermetrópico periférico en un ojo miope corregido (41): 3 Según Smith et al. (42), el desenfoque hipermetrópico impuesto experimentalmente, que es común en los ojos miopes corregidos, puede aumentar el crecimiento ocular; mientras que el desenfoque miope, especialmente cuando se impone sobre un área grande de la retina, puede retrasar el alargamiento axial. El patrón de refracción periférica varía con la refracción central. Las personas con miopía suelen tener hipermetropía relativa en la periferia, mientras que las personas con hipermetropía tienen miopía relativa en la periferia (43,44).
- Trabajo intensivo de cerca (45,46): Ghosh et al. (45) sugirieron que el mecanismo por el cual el trabajo cercano aumenta la longitud axial es la influencia combinada de factores biomecánicos (es decir, fuerzas musculares extraoculares, contracción del músculo ciliar) asociados con tareas cercanas en la mirada hacia abajo.
- Tiempo al aire libre (47): I. Morgan informó a la reunión que la epidemia de miopía en el este de Asia se debe principalmente a los cambios en los factores ambientales (sociales), específicamente la educación intensiva y el menor tiempo al aire libre (Fig. 6). La variación estacional observada en la progresión de la miopía agrega peso al argumento de que el tiempo que se pasa al aire libre ralentiza la progresión de la miopía.
- Desenfoque hipermetrópico sucesivo y simultáneo: dado que las escenas en interiores tienen una topografía dióptrica muy heterogénea, es más probable que los ojos experimenten un desenfoque hipermetrópico, que ha demostrado ser un fuerte estímulo para el crecimiento miope en animales de laboratorio (49).
Genética e historial parental
La genética y el medio ambiente juegan un papel en el desarrollo y la progresión de la miopía, pero la contribución genética se considera pequeña, y existe consenso en que los genes pueden determinar la susceptibilidad a los factores ambientales (50).
Los genes para la miopía y el alto desarrollo de miopía se han identificado en estudios familiares y estudios de gemelos y mediante análisis de ligamiento. Estos estudios han demostrado que la genética puede explicar el 60–80% de la varianza en el error de refracción esférico equivalente y la longitud axial. Sin embargo, otros estudios han indicado que la contribución genética es mucho menor y no explica la mayoría de los casos de miopía alta (53). Los estudios sobre la contribución genética deben incluir la evaluación de los aspectos ambientales, ya que factores como el tiempo que pasan al aire libre y cerca del trabajo varían según la familia, pues el rápido aumento en la prevalencia de la miopía que se observa durante un corto tiempo en el este de Asia no puede explicarse por la genética, lo que indica que los factores ambientales asociados con una educación y urbanización más generalizadas juegan un papel más importante.
Control de miopía
Se han evaluado varios enfoques ópticos para el control de la progresión de la miopía en las últimas décadas. Estos se basan en diferentes hipótesis de progresión de la miopía. Los detalles de estos métodos ópticos se resumen a continuación.
Métodos de espectáculo
– Dejar la miopía sin corregir no redujo la tasa de progresión en comparación con la corrección completa o la corrección insuficiente en un estudio aleatorizado prospectivo de 12 meses en niños de 9 a 12 años (65). Se ha demostrado que la corrección insuficiente aumenta la progresión de la miopía, por lo no se recomienda (67).
– Se ha demostrado que las lentes de adición progresiva tienen un efecto pequeño (68). La reducción en la tasa de progresión de la miopía se correlacionó con el grado de miopía relativa producida en la retina superior por una adición cercana (69).
– Los lentes bifocales ejecutivos con una adición de +1.50 y un prisma de base 3 D redujeron la tasa de progresión de la miopía en un 57% después de tres años (62). Se cree que estas lentes reducen el estímulo para el alargamiento axial, ya sea reduciendo el retraso acomodativo en la miopía (aunque esta asociación aún no se ha demostrado) o imponiendo un enfoque miope en la retina periférica superior.
– Se investigaron lentes con periférico plus que están destinados a reducir el grado de desenfoque hipermetrópico periférico relativo en personas con miopía en un ensayo de 12 meses. La reducción en la progresión de la miopía no fue estadísticamente significativa.
Métodos con lentes de contacto
– Las lentes estándar rígidas gas-permeables no reducen la tasa de alargamiento axial miope y pueden conducir a un aplanamiento corneal (72).
– Las lentes de contacto bifocales reducen significativamente la tasa de progresión de la miopía, tanto en términos del equivalente esférico del error de refracción como de la longitud axial. Se ha sugerido que las lentes de contacto bifocales actúan reduciendo el retraso acomodativo (73); sin embargo, es más probable que actúen reduciendo el desenfoque hipermetrópico periférico o imponiendo el desenfoque miope (74). La corrección del desenfoque periférico mediante lentes de contacto periféricos plus da como resultado una reducción del 50% en la tasa de progresión miope, en términos de equivalente esférico y longitud axial (75).
– Una lente de contacto de doble enfoque con múltiples anillos de potencia adicional que produce un desenfoque miope relativo en una gran parte de la retina resultó en una reducción del 36% en la progresión de la miopía y una reducción del 49% en la tasa de cambio en la longitud axial: sin embargo, aún se requieren estudios a largo plazo (41).
– La ortoqueratología implica el uso de lentes rígidas gas permeables durante la noche para aplanar la córnea. El uso de estas lentes condujo a una reducción constante en la progresión de la miopía de aproximadamente 45% durante un período de dos años y 30% durante cinco años, cuando se mide en términos de longitud axial (63).
– Las lentes de profundidad de enfoque extendida respaldan la hipótesis del desenfoque miope al reducir las señales que se cree que aumentan el crecimiento axial (76). Los resultados preliminares mostraron una reducción del 35% en la tasa de progresión del equivalente esférico del error de refracción y una reducción de hasta el 45% en la tasa de progresión en la longitud axial.
Tiempo al aire libre e influencias conductuales
Se han realizado varios estudios para determinar los efectos de la cantidad de tiempo que se pasa al aire libre y los cambios de comportamiento en la progresión de la miopía en niños (77, 78, 79). Están surgiendo pruebas de que pasar más tiempo al aire libre puede proteger contra la aparición de la miopía, el efecto del trabajo cercano y el efecto de la miopía de los padres y posiblemente ralentizar la tasa de progresión de la miopía.
Se informó que, cuando los niños pasan suficiente tiempo al aire libre (más de dos horas / día), el riesgo de miopía se reduce, incluso cuando tenían dos padres miopes y continuaban realizando trabajos cerca del trabajo (77). El tiempo total que se pasa al aire libre parece ser el factor importante.
El mecanismo de acción del tiempo que se pasa al aire libre sigue siendo desconocido y requiere más investigación. Se ha planteado la hipótesis de que la luz más brillante al aire libre estimula la liberación de dopamina desde la retina, que según se informa inhibe el alargamiento axial en modelos animales de miopía de privación de forma (81, 82). Las diferencias estacionales en las tasas de progresión miope, que son más rápidas en invierno y más lentas en verano, respaldan esta hipótesis (83). Se deben realizar más estudios sobre el efecto del tiempo que se pasa al aire libre, con métodos de encuesta mejores y más simples.
Control farmacológico y terapéutico
Se han investigado varias intervenciones terapéuticas para el control de la miopía. El uso de atropina al 0.01% es el régimen de tratamiento más común para el manejo de la miopía en niños en varios países asiáticos. Una intervención experimental que se está probando en Dinamarca es la 7-metilxantina; parece prometedor, pero su seguridad a largo plazo aún necesita ser estudiada.
– Atropina: La atropina reduce la progresión de la miopía en niños de una manera relacionada con la dosis, pero se produce un efecto de rebote (“recuperación”) con dosis más altas (85). Las gotas oculares de atropina generalmente se consideran seguras, aunque en un alto porcentaje tiene efectos secundarios sustanciales (reacciones alérgicas, pupilas dilatadas fijas, parálisis acomodativa, conjuntivitis papilar y, en algunos casos, náuseas y vómitos). Dosis más bajas, como 0.01% (en oposición a la concentración clínica habitual de 1.0%), reducen los efectos secundarios comunes observados con la dosis más alta, incluyendo dilatación de la pupila, pérdida de acomodación y visión cercana reducida. La atropina al 0.01% resultó en una reducción del 59% en la tasa de progreso de la miopía, con efectos adversos mínimos; sin embargo, de forma controvertida, no tuvo ningún efecto sobre el alargamiento axial (85). Durante un período de observación de siete años después del tratamiento durante dos años, la atropina al 0.01% desaceleró la progresión de la miopía en un 50% en niños de 6 a 9 años, sin efecto aparente sobre las tasas de alargamiento axial.
Se necesitan pautas clínicas sobre quién debe ser tratado, cuándo debe comenzar el tratamiento y el cese y la duración del tratamiento. Las gotas para los ojos de atropina fueron aprobadas recientemente por la FDA de los Estados Unidos para la terapia de ambliopía a largo plazo en niños. Actualmente no hay aprobación regulatoria para el uso de atropina para retrasar la progresión de la miopía.
–Metilxantina: Es un antagonista no selectivo de la adenosina que afecta la liberación de neurotransmisores (86). Se cree que la 7-metilxantina penetra la barrera hematoencefálica solo mínimamente y es relativamente no tóxica; Se excreta predominantemente a través de los riñones. Durante ocho años de seguimiento de 750 niños daneses miopes que fueron tratados con varias dosis sistémicas de 7-metilxantina, no se informaron efectos secundarios. La dosis de 400 mg dos veces al día redujo la progresión de la miopía y el alargamiento excesivo del ojo en un 60% (70).
Investigación (Conclusiones y acuerdos)
A la vista de los anteriores datos expuestos y analizados se puso de manifiesto que las áreas donde se requiere más investigación para mejorar el manejo basado en la evidencia eran las siguientes:
- EPIDEMIOLOGÍA DE LA MIOPÍA: Los estudios epidemiológicos son esenciales para definir prioridades en la planificación y focalización de recursos para el cuidado de la vista. El manejo de la miopía y la prevención de la discapacidad visual por miopía no corregida deben optimizarse en vista de los aumentos proyectados en la prevalencia global de la afección. Los participantes acordaron que la DMM debería incluirse en estudios epidemiológicos sobre la prevalencia y las causas de la discapacidad visual, incluidas las evaluaciones rápidas de ceguera evitable y las encuestas de la OMS sobre la discapacidad visual y sus causas.
- FACTORES AMBIENTALES: Deben idearse estrategias para aumentar la cantidad de tiempo que los niños pasan al aire libre, particularmente en preescolar y primaria. Aunque se desconoce el aspecto que imparte un efecto protector. Los posibles roles de la iluminación ambiental y las diferencias en la composición espectral de la luz, la topografía dióptrica y la escala espacial deben aclararse para optimizar cualquier beneficio terapéutico.
- ENFOQUES ÓPTICOS Y FARMACEUTICOS: Se deben realizar ensayos clínicos de mejores prácticas (ensayos aleatorios y/o ciegos, con potencia y uso adecuados de agentes ciclopléjicos, durante un mínimo de 12 meses y preferiblemente más) para optimizar las estrategias.
- TRABAJO DE CERCA: Es ampliamente reconocido que el trabajo de cerca en la educación formal está asociado con la miopía. Se deben realizar estudios para identificar y caracterizar los componentes que podrían causar miopía.
- TERAPIA COMBINADA: Se desconoce el efecto de combinar los diversos tipos de estrategias preventivas y de control. Es importante saber cómo funcionan juntas las diferentes terapias y estrategias, ya que es poco probable que los pacientes usen un método de forma aislada.
- FACTORES DE RIESGO Y HETEROGENEIDAD INDIVIDUAL: Es probable que las diferencias individuales en la susceptibilidad y el comportamiento desempeñen un papel en la determinación de la aparición de miopía y, probablemente, el grado máximo de miopía. Hay brechas significativas en la comprensión del desarrollo refractivo desde aproximadamente los dos años de edad hasta el comienzo de la educación formal y entre el final de la educación secundaria y la mediana edad (aproximadamente 40 años). Se alientan los estudios sobre el desarrollo refractivo y la prevalencia de errores refractivos desde aproximadamente los dos años hasta los 25 años inclusive. Estos se beneficiarían de los métodos para documentar el comportamiento cuantitativamente, como la validación de cuestionarios y la medición objetiva de la exposición a la luz.
- ALTA MIOPÍA, MIOPÍA PATOLÓGICA Y AFECCIONES COMÓRBIDAS: No se entiende si la miopía alta se convierte en miopía patológica o si son dos afecciones con diferentes causas subyacentes. Se necesitan estudios retrospectivos de casos y controles, estudios poblacionales o metaanálisis para determinar si y qué proporción de personas con miopía alta desarrollan miopía patológica. Se debe estudiar la historia natural, incluida la edad de inicio de la miopía patológica, y los factores de riesgo y los factores asociados con la discapacidad visual. Se deben identificar las causas de la miopía alta y la miopía patológica, incluida la genética y el medio ambiente, cerca del trabajo y el tiempo que se pasa al aire libre. Se desconoce la proporción de personas con miopía que desarrollarán complicaciones oculares, ni la edad o el nivel de miopía en el que generalmente se desarrollan complicaciones. Se requiere investigación para comprender las causas de las condiciones comórbidas asociadas con la miopía y sus factores de riesgo
- EXÁMENES OCULARES EN MIOPÍA: El uso de agentes ciclopléjicos en los exámenes oculares debe estandarizarse, ya que no existen pautas sobre el uso de estos agentes en la miopía. Los estudios muestran que el nivel medido de error de refracción en personas con miopía difiere cuando se usan ciclopléjicos. Se requieren estudios para determinar el régimen ciclopléjico óptimo para estudiar la progresión de la miopía en niños y adultos de diferentes orígenes étnicos, incluido el agente ciclopléjico, la concentración (número de gotas) y el tiempo antes de la medición.
Conclusiones generales
Los aumentos documentados en la prevalencia de miopía y alta miopía en todo el mundo son un grave problema de salud pública. Los datos para informar la investigación, la práctica clínica y la política de salud pública deben producirse con urgencia. Los participantes en esta consulta conjunta acordaron recomendaciones para el uso consistente de la terminología internacional para obtener datos precisos y comparables internacionalmente sobre la prevalencia de miopía y miopía alta. Acordaron las definiciones de miopía y miopía alta y una descripción de las consecuencias patológicas de la miopía. Además, acordaron que la miopía y la miopía alta deberían incluirse como causas atribuibles de discapacidad visual en las encuestas epidemiológicas, y que el término “degeneración macular miópica” debería usarse para clasificar las enfermedades retinianas cegadoras asociadas con la miopía alta, en lugar de los muchos otros términos en uso actual.
La consulta brindó la oportunidad de clasificar los defectos miopes, evaluar la evidencia sobre las estrategias de control de la miopía e identificar lagunas en el conocimiento que deben llenarse urgentemente como base para estrategias basadas en la evidencia para reducir la prevalencia de miopía alta y la discapacidad visual asociada.
PUBLICADO por la OMS «Report: the impact of myopia and high myopia »
1. Bourne RR, Stevens GA, White RA, Smith JL, Flaxman SR, Price H et al. Causes of vision loss worldwide, 1990-2010: a systematic analysis. Lancet Global Health. 2013;1:e339–e349.
2. Holden B, Fricke TR, Wilson DA, Jong M, Naidoo KS, Sankaridurg P et al. Global prevalence of myopia, high myopia, and temporal trends from 2000 to 2050 (in preparation).
10. International statistical classification of diseases and related health problems, 10th revision, version for 2010. Geneva: World Health Organization; 2010.
11. Resolution WHA66.4. Universal eye health. A global action plan 2014–2019. In: Sixty-sixth World Health Assembly, Geneva, 20–27 May 2013. Resolutions and decisions, annexes. Geneva: World Health Organization; 2013:5 (WHA66/2013/REC/1; http://apps.who.int/gb/ebwha/pdf_files/WHA66-REC1/WHA66_2013_REC1_complete.pdf).
12. World urbanization prospects: the 2014 revision (document ST/ESA/SER.A/366). New York: United Nations, Department of Economic and Social and Economic Affairs, Population Division; 2014 (http://esa.un.org/unpd/wup/).
41. Sankaridurg P, Holden B, Smith E III, Naduvilath T, Chen X, de la Jara PL et al. Decrease in rate of myopia progression with a contact lens designed to reduce relative peripheral hyperopia: one-year results. Invest Ophthalmol Vis Sci. 2011;52:9362–7.
42. Smith EL III, Hung LF, Arumugam B. Visual regulation of refractive development: insights from animal studies. Eye. 2014;28:180–8.
45. Ghosh A, Collins MJ, Read SA, Davis BA, Chatterjee P. Axial elongation associated with biomechanical factors during near work. Optom Vis Sci. 2014;91:322–9.
46. Woodman EC, Read SA, Collins MJ, Hegarty KJ, Priddle SB, Smith JM et al. Axial elongation following prolonged near work in myopes and emmetropes. Br J Ophthalmol. 201;95:652–6.
47. Lin Z, Vasudevan B, Jhanji V, Mao GY, Gao TY, Wang FH et al. Near work, outdoor activity, and their association with refractive error. Optom Vis Sci. 2014;91:376–82.
49. Flitcroft DI. The complex interactions of retinal, optical and environmental factors in myopia aetiology. Progr Retinal Eye Res. 2012;31:622–60.
50. Lim LT, Gong Y, Ah-Kee EY, Xiao G, Zhang X, Yu S. Impact of parental history of myopia on the development of myopia in mainland China school-aged children. Ophthalmol Eye Dis. 2014;6:31–5.
62. Cheng D, Woo GC, Drobe B, Schmid KL. Effect of bifocal and prismatic bifocal spectacles on myopia progression in children: three-year results of a randomized clinical trial. JAMA Ophthalmol. 2014;132:258–64.
63. Si JK, Tang K, Bi HS, Guo DD, Guo JG, Wang XR. Orthokeratology for myopia control: a meta-analysis. Optom Vis Sci. 2015;92:252–7.
65. Li SM, Li SY, Liu LR, Guo JY, Chen W, Wang NL et al. Full correction and undercorrection of myopia evaluation trial: design and baseline data of a randomized, controlled, double-blind trial. Clin Exp Ophthalmol.
2013;41:329–38.
67. Chung K, Mohidin N, O’Leary DJ. Undercorrection of myopia enhances rather than inhibits myopia progression. Vis Res. 2002;42:2555–9.
68. Berntsen DA, Sinnott LT, Mutti DO, Zadnik K. A randomized trial using progressive addition lenses to evaluate theories of myopia progression in children with a high lag of accommodation. Invest Ophthalmol Vis Sci. 2012;53:640–9.
69. Berntsen DA, Barr CD, Mutti DO, Zadnik K. Peripheral defocus and myopia progression in myopic children randomly assigned to wear single vision and progressive addition lenses. Invest Ophthalmol Vis Sci. 2013;54:5761–70.
70. Trier K, Munk Ribel-Madsen S, Cui D, Brogger Christensen S. Systemic 7-methylxanthine in retarding axial eye growth and myopia progression: a 36-month pilot study. J Ocul Biol Dis Inform. 2008;1:85–93.
72. Grosvenor T, Perrigin D, Perrigin J, Quintero S. Rigid gas-permeable contact lenses for myopia control: effects of discontinuation of lens wear. Optom Vis Sci. 1991;68:385–9.
73. Aller T. Results of a one-year prospective clinical trial (CONTROL) of the use of bifocal soft contact lenses to control myopia progression. Ophthal Physiol Optics. 2006;26(Suppl 1):8.
74. Walline JJ, Greiner KL, McVey ME, Jones-Jordan LA. Multifocal contact lens myopia control. Ophthalmol Vis Sci. 2013;90:1207–14.
75. Holden B, Sankaridurg P, Smith E, Aller T, Jong M, He M. Myopia, an underrated global challenge to vision: where the current data takes us on myopia control. Eye. 2014;28:142–6.
76. Bakaraju R, Xu P, Chen X, Ma M, Song S, Jong M et al. Extended depth-of-focus contact lenses can slow the rate of progression of myopia. Abstract. Annual meeting, Imaging the eye, Denver, Colorado. Rockville, MD: Association for Research in Vision and Ophthalmology Inc.; 2015.
77. Rose KA, Morgan IG, Ip J, Kifley A, Huynh S, Smith W et al. Outdoor activity reduces the prevalence of myopia in children. Ophthalmology. 2008;115:1279–85.
78. Jones LA, Sinnott LT, Mutti DO, Mitchell GL, Moeschberger ML, Zadnik K. Parental history of myopia, sports and outdoor activities, and future myopia. Invest Ophthalmol Vis Sci. 2007;48:3524–32.
79. Wu PC, Tsai CL, Wu HL, Yang YH, Kuo HK. Outdoor activity during class recess reduces myopia onset and progression in school children. Ophthalmology. 2013;120:1080–5.
81. Ashby RS, Schaeffel F. The effect of bright light on lens compensation in chicks. Invest Ophthalmol Vis Sci. 2010;51:5247–53.
82. Smith EL, Hung L-F, Huang J. Protective effects of high ambient lighting on the development of formdeprivation myopia in rhesus monkeys. Invest Ophthalmol Vis Sci. 2012;53:421–8.
83. Gwiazda J, Deng L, Manny R, Norton TT, Group CS. Seasonal variations in the progression of myopia in children enrolled in the Correction of Myopia Evaluation Trial. Invest Ophthalmol Vis Sci. 2014;55:752–8.
85. Chia A, Chua WH, Cheung YB, Wong WL, Lingham A, Fong A et al. Atropine for the treatment of childhood myopia: safety and efficacy of 0.5%, 0.1%, and 0.01% doses (Atropine for the Treatment of Myopia 2).
Ophthalmology. 2012;119:347–54.
86. Bullock S, Manias E. Fundamentals of pharmacology. London: Pearson Higher Education; 2013.